Аш-эс диаграмма или диаграмма h, s (может называться она и диаграмма Молье) представляет собой определение состояния тепловых и физических свойств жидкого и газообразного вещества. В качестве вещества вода рассматривается как жидкость, пар рассматривается как газообразное вещество. Для воды и водяного пара существует специально разработанная диаграмма, она показывает, как изменяются разные свойства в соответствии с параметрами. H, s схема — популярная и самая используемая в области исследования воды, тогда как эта жидкость — самый доступный, недорогой материал, на который обращается пристальное внимание. Более внимательно относятся к образованию пара, потому что в состоянии жидкости вода почти не сжимается.
Создание диаграммы требуется в теплоэнергетической отрасли в первую очередь. С ее помощью подбирается эффективное и надежное оборудование для тепловых процессов на основе пара. Он при этом образуется из воды, а она в свою очередь проявляет свои теплофизические свойства. Исследует такая схема изменение давления и температуры. Исследования воды, в которых H2O выступала, как главный компонент, проводились годами и на международном уровне. Разные страны сотрудничали и активно внедряли свои наработки. Были созданы особые нормативные документы, где с помощью уравнений производились описания свойств воды в ее жидком виде и пара в форме газообразного вещества. Специальные таблицы тоже отражают соответствующие данные. Уравнения же используются как для общего применения, так и для научного. Они соответствуют Системе международных уравнений. Таблицы были опубликованы в массы и используются в расчетной практике тепловой инженерии. Еще во времена СССР термодинамические свойства воды, которая постоянно была в центре событий (вспомнить нужно и Вукаловича), просчитывались при помощи таблиц. Динамическую вязкость также отражала диаграмма, которая в точности соответствовала таблице.
Схема Молье
Немецкий ученый из Германии Рихард Молье был известным теплотехником и занимал свою исследовательскую нишу в обществе. Он окончил Высшую техническую школу г. Дрездена и получил профессорскую степень. Основными его исследованиями были процессы превращения вещества и энергии. Водяной пар был главным источником его работы. На основе этого ученый написал книгу про таблицы и диаграммы водяного пара. В 1994 году была создана диаграмма, помогающая упростить решения задач на практике в сфере теплотехники, где основными координатами стали энтальпия – h и энтропия (s).
Единица h это потенциал термодинамики, он показывает изменение состояния системы в равновесии, с использованием давления и частиц как независимых переменных. Одним словом это энергия, требуемая для получения теплоты, когда давление находится в одной поре. Энтропией называется превращение, этот термин очень часто используется в точных науках. Он введен в понятии термодинамика и термодинамическая система. После издания книги диаграмму назвали диаграммой Молье. I, ее называли изначально, пока она не поучила название h, s схема.
Структурированная система диаграммы
Она содержит в себе понятия воды и пара. Рассматривая понятия с точки зрения теплотехники, они достаточно интересные.
Сухость определена параметром x, который показывает массовую долю пара. Чаще всего понимают под этим насыщенное вещество. Значение показателя, равное нулю, становится в момент закипания воды, полного насыщения. Если значение единица, то среди жидкости и газообразного состояния пар присутствует, а H2O нет совсем. При внесении состояния воды, она определена одной точкой, при внесении в таблицу пара, который определен другой точкой, достаточно их соединить, чтобы получить кривую сухости. Нулевой икс — это нижняя граница, а единичный икс это верхняя граница. Та область между кривыми означает насыщенность влажного пара. Область ниже обозначает показатель воды, направленный от икса практически по прямой. Область над икс единица обозначает перегретый водяной газ.
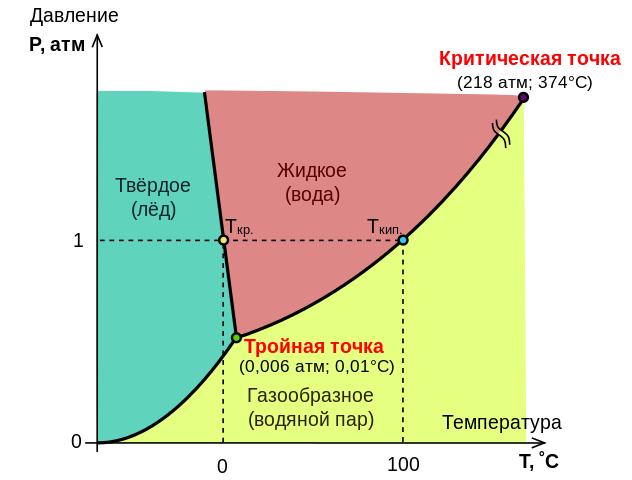
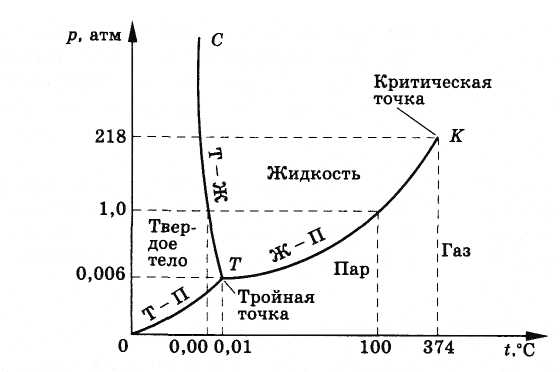
Точка критического состояния определена буквой K. Если давление высокое, критическое, оно доводит воду и пар до идентичного состояния. Понятия жидкости и газообразного состояния просто исчезают в данном случае. Критическое состояние воды обозначается критической точкой.
Изотерма – это линия, выстроенная путем объединения энтальпии и энтропии в определенных температурах.
Адиабатный процесс широко рассмотрен в турбинах и паровых машинах, где очень быстро происходит теплообменный процесс с внешней средой. Обратимым процессом в этих машинах является адиабата.
Изохорный процесс происходит при теплообмене водяного пара, который находится в сосуде.
Как используется диаграмма состояния вода пар
Диаграммы рассматриваемого типа применяются, чтобы рассчитывать испарение в системах охлаждения. Зачастую наблюдается применение диаграмм в системах кондиционирования, с ее помощью легко определить относительную и абсолютную влажность при изменении температурного режима. Схема помогает рассчитывать влажность воздуха при определенной температуре. Существует и электронная версия диаграммы, показывающей соответственно те же самые состояния. Пользоваться электронной диаграммой проще, открывается окно, куда вводятся все данные в определенные графы.
Идеальные газы рассчитывают с помощью специального уравнения p·v=R·T. Насыщенные пары и идеальные газы отличаются по свойствам. Определить параметры насыщенных паров сложнее, чем идеального газа. Самым простейшим уравнением для определения состояния пара признается уравнение Новикова и Вукаловича, высчитывать по ним нелегко. Диаграммы и таблицы для газообразного H2O используются только потому, что пар не подчинен законам для идеальных газов. Схема не только определяет точные параметры воды, но оценивает ее изменения, что очень удобно. Схема отражает фазовые изменения, показывает их графически.
Когда начинающие исследователи видят диаграмму состояния воды и пара, они немного ужасаются и пугаются той миллиметровой паутине, которая представлена на ней. Содержание влаги в воздухе называется влагосодержанием. На диаграмме эта величина показана в г/кг, т.е. сколько пара или газообразной воды находится в воздухе. Современные компьютеры очень просто справляются со сложными процессами составления диаграмм, где все параметры определены специальными программами. Паровые процессы наглядно представлены в таблице и диаграмме, все видно от и до. Прочитать вроде бы запутанную паутину не сложно, если знать основные понятия, их изменение и функциональное состояние.
Практические расчеты проводятся по неполной диаграмме, рассматривалась в первую очередь область, относящаяся к пару. Эта область находится справа от критической точки, где определен влажный и перегретый пар. Графическая схема позволяет сравнивать разные величины и при теоретическом ответе схема играет очень важную роль в определении параметров и функций водяного и влажного пара. H, s схема делает процессы расчетов проще, является незаменимым на предприятии, которое работает с подобной системой расчетов.